Chapitre 1 : L’origine du génotype des individus
Diaporama chap 1Révision : TD la conservation des génomes
Term spé SVT. Test 1. Génétique.
Rappels
Term spé SVT. Test 2.
Génétique. La notion de clone
Term spé SVT. Test 3.
Génétique. La lignée clonale.
Term spé SVT. Test 4.
Génétique. Les lois de Mendel.
Term spé SVT. Test 5.
Génétique. Méiose et brassage
Term spé SVT. Test 6.
Génétique. Lien entre les gènes.
Term spé SVT. Test 7.
Génétique. Maladies génétiques
Term spé SVT. Test 8.
Génétique. Les accidents
génétiques.
Dans le monde
vivant, une grande diversité de
phénotypes est observable : à l’échelle
de l’espèce, de l’écosystème (2nde).
Les mutations contribuent pour une part à cette diversité
en formant de
nouveaux allèles d’un gène (1èreSpé).
La reproduction sexuée joue
également un rôle essentiel car à chaque
génération elle réalise un brassage
génétique à l’origine d’individus
uniques.
Lors du passage
d’une génération à une autre par
reproduction sexuée, on constate que les caractères
spécifiques de l’espèce
sont conservés. Ces caractères sont
déterminés par les gènes répartis sur les
chromosomes. La conservation des caractères de
l’espèce dépend donc des
mécanismes qui participent à la transmission des
chromosomes d’une génération à
l’autre.
Plusieurs activités peuvent être réalisées en ligne pour réactiver certaines notions de spécialité première :
- Réviser les étapes de la méiose
- Revoir comment on obtient un caryotype
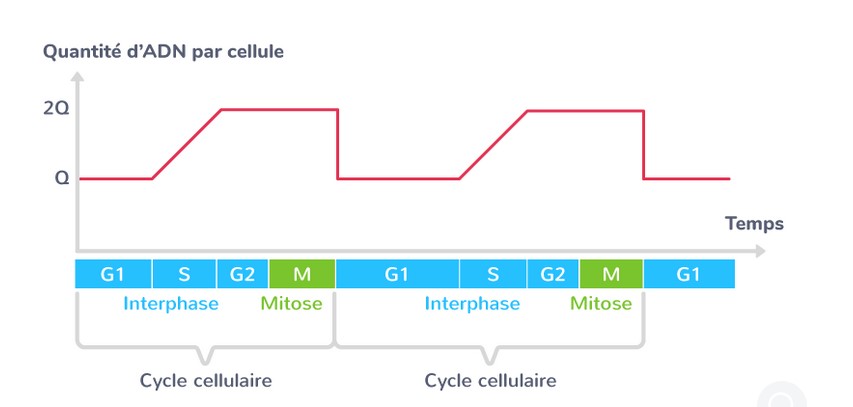
- Réviser les états des chromosomes au cours du cycle cellulaire
Comment la reproduction sexuée permet-elle à la fois le maintien des caractéristiques de l’espèce et participe également à la diversification du vivant ?
I.
La
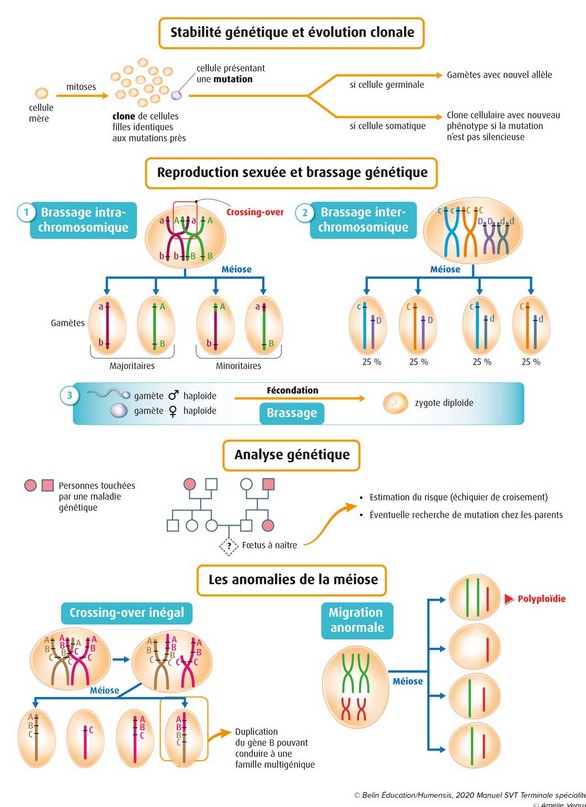
conservation des génomes : stabilité
génétique
et évolution clonale
Un individu est
constitué de cellules qui
résultent de mitoses à partir
d’une cellule-œuf initiale. Ce processus
de
multiplication permet d’obtenir un ensemble de cellules en
théorie
génétiquement identiques, c’est-à-dire un clone,
puisque la mitose est précédée d’un
mécanisme efficace de copie de
l’information génétique, la réplication de
l’ADN.
Cependant,
cette copie de l’ADN n’est pas
totalement fiable : on estime que le taux
d’erreur est de 1 pour 109 nucléotides
copiés, à l’origine des mutations.
En prenant en compte la
taille du génome humain (6,4 x 109 paires de
nucléotides) ainsi que
le nombre de divisions qui ont lieu au cours d’une vie humaine
(estimé à 1017),
on peut affirmer qu’il existe une diversité
génétique chez les cellules constituant un individu.
B.
Un
individu : une mosaïque de
sous-clones génétiquement différents
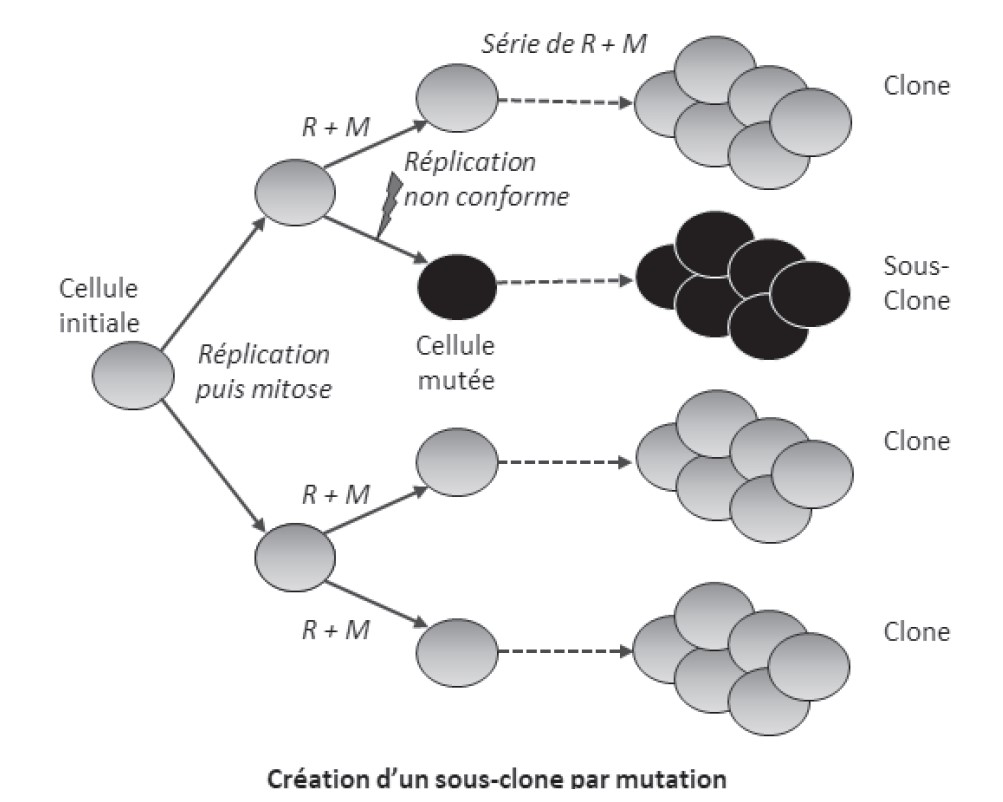
Chaque individu est donc constitué d’une mosaïque de clones présentant de faibles variations génétiques liées à ces mutations accumulées. Ces clones sont constitués de cellules séparées (cas des cellules sanguines) ou de cellules restant associées. Les mutations et autres accidents génétiques affectant une cellule deviennent pérennes pour toute la lignée cellulaire qui dérive du mutant, formant ainsi un sous-clone particulier.
II.
Le
brassage des génomes assuré par la reproduction
sexuée à chaque génération
La
fécondation est la fusion de deux gamètes apportant
chacun un lot haploïde (n) de chromosomes.
La cellule-œuf
qui en résulte est donc diploïde
(2n).
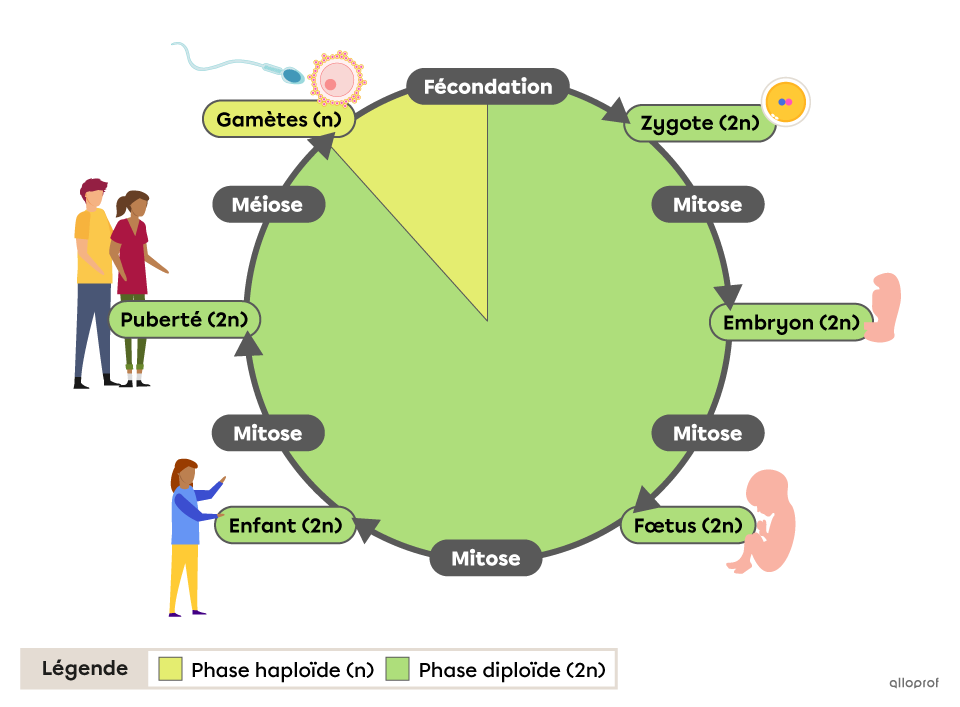
Document : cycle de vie d'un animal
- A.
Fécondation
et diversification du
génome
L’observation des états de caractère au sein d’une famille nous indique que la reproduction sexuée, grâce à la formation de gamètes (méiose) et leur rencontre aléatoire (fécondation) permet de générer des individus aux phénotypes différents.
-

L’expression d’un caractère gouverné par un gène est le résultat de l’interaction des deux allèles de ce gène qui se rencontrent lors de la fécondation. Ces allèles peuvent être identiques (= homozygote) ou différents (= hétérozygote). L’expression du phénotype résulte alors des relations de dominance et de récessivité des allèles.
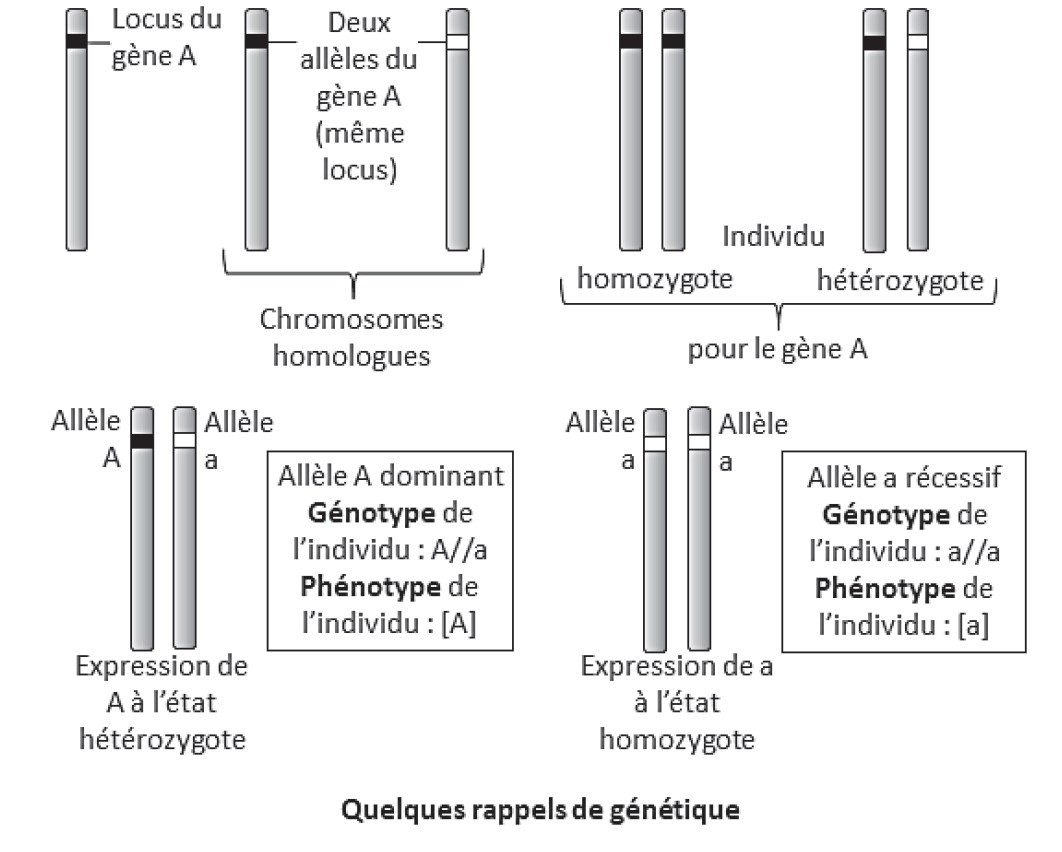

B. Mendel, une première approche de la génétique-
Un croisement de deux individus de lignée pure (homozygotes) différant pour un seul caractère aboutit à l’obtention d’une première génération homogène de même phénotype (F1) et permet de définir les relations de dominance et de récessivité entre les allèles qui sont apportés de manière indépendante par les gamètes lors de la fécondation.

Document
: La formation
des gamètes à partir de deux génotypes
(gènes indépendants)
L’observation
des phénotypes de drosophiles
différant par deux caractères à l’issue
d’un croisement test (F1 x homozygote
récessif) révèle l’apparition de
deux nouveaux phénotypes qualifiés de
« recombinés » et témoignant
d’une nouvelle association d’allèles,
différente de celle observée chez les
parents : on parle de brassage
allélique.
Le comptage et
le calcul des proportions des
phénotypes résultant de ce croisement test permet de
savoir si les gènes sont
liés, c’est-à-dire situés sur le même
chromosome ou non. Si les deux gènes
considérés sont portés par des paires
de
chromosomes différentes, le résultat du test cross
présente 4 phénotypes équiprobables
(50% de phénotypes parentaux et 50%
de phénotypes recombinés). De tels
résultats s’expliquent par une répartition
aléatoire des chromosomes de
chaque paire au cours de l’anaphase I de méiose :
on parle de brassage
allélique interchromosomique.
Le nombre de combinaisons génétiques possibles dans les gamètes résultant de ce brassage allélique est d’autant plus élevé que le nombre de gènes à l’état hétérozygote est plus grand chez les parents : pour n paires de chromosomes, un individu peut former 2n gamètes différant par leur assortiment de chromosomes.
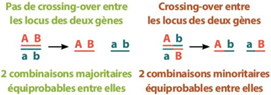
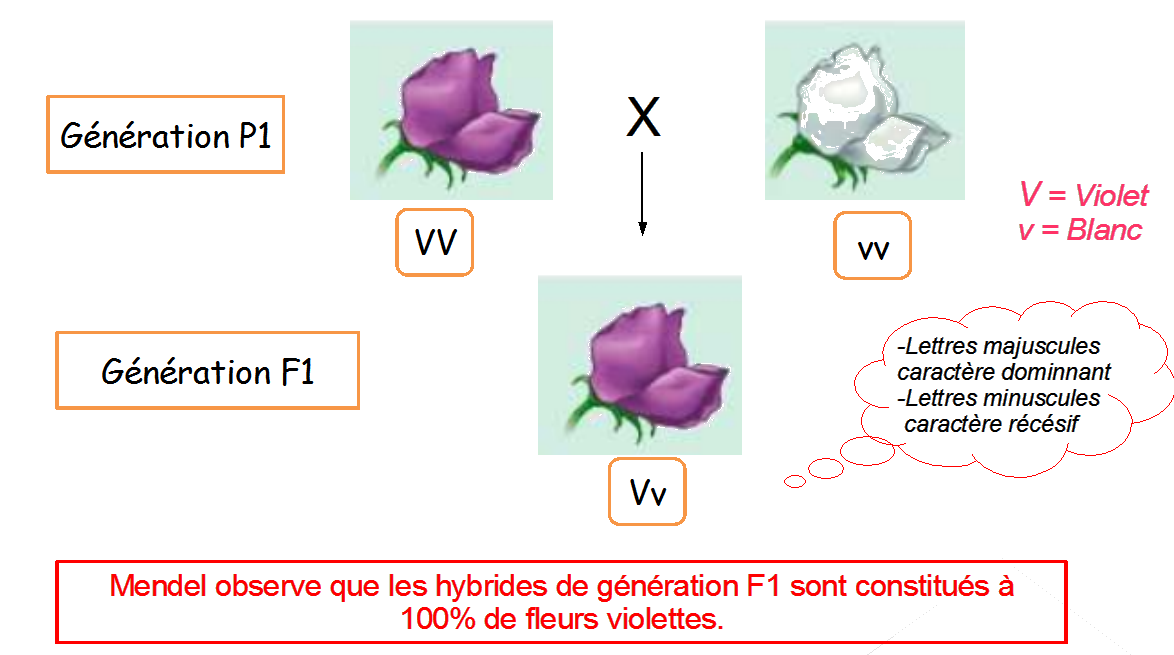
Première loi : Loi d’uniformité des hybrides de première génération (tous les hybrides de F1 sont 100% identiques)
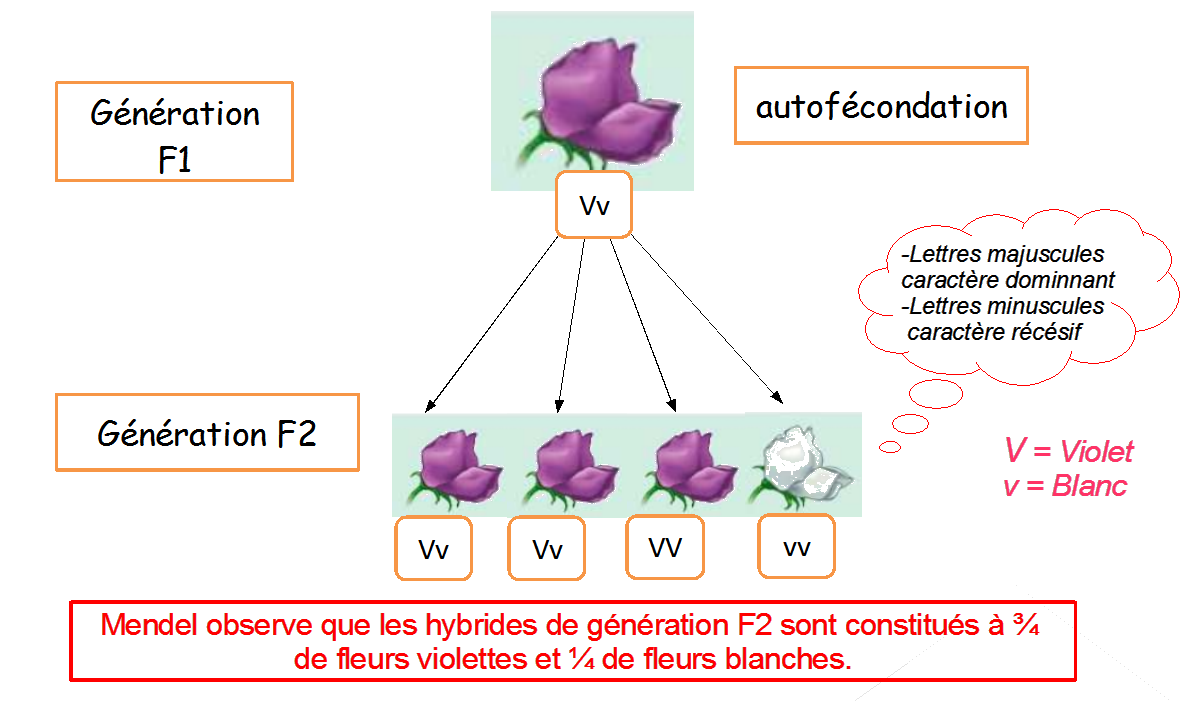
Deuxième loi : Loi de disjonction des allèles (1 caractère ne s’étant pas exprimé lors de la 1ère génération peut s’exprimer à la seconde génération)

C.
Des
cas échappant aux lois de
l’hérédité de Mendel
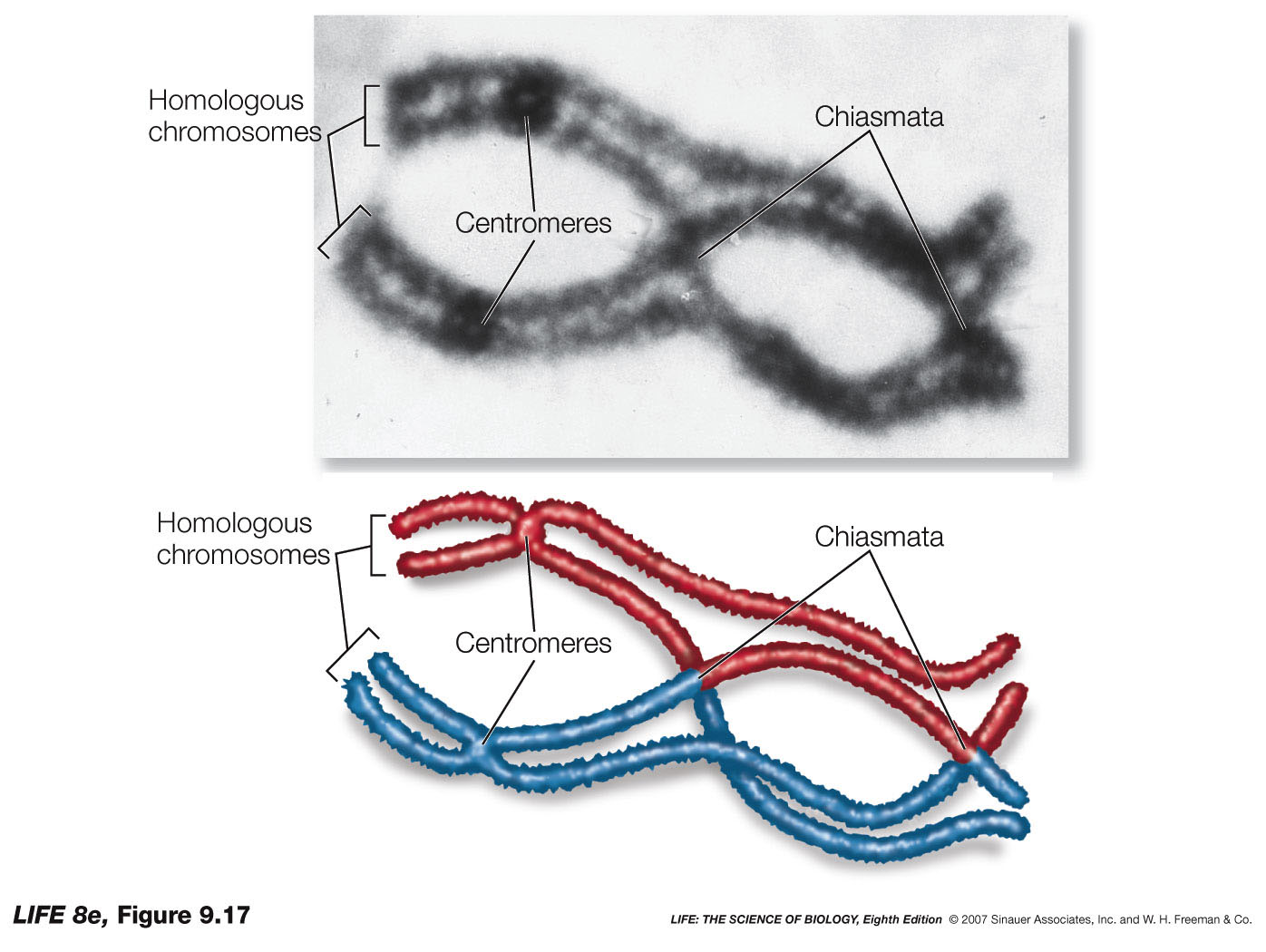
Ce
mécanisme est appelé crossing-over,
est
aléatoire quant à sa localisation et permet
l’échange d’allèles entre deux
chromosomes homologues. On parle de brassage
allélique intrachromosomique. Ce n’est pas une
anomalie : il se
produit fréquemment
et contribue de manière très importante à a
diversité génétique des individus.

La méiose
est donc à l’origine d’un double
brassage génétique : pour chaque gène
à l’état hétérozygote, chaque
cellule issue de la méiose recevra au hasard un seul des deux
allèles présents,
les combinaisons obtenues étant d’autant plus nombreuses
que le nombre de gènes
à l’état hétérozygote est
élevé.
Ce mécanisme génétique joue alors un rôle essentiel dans l’évolution biologique, en permettant par exemple la vision trichromatique de certains primates.
L’observation de caryotypes présentant un nombre différent de chromosomes permet de mettre en évidence d’autres particularités méiotiques, souvent létales.
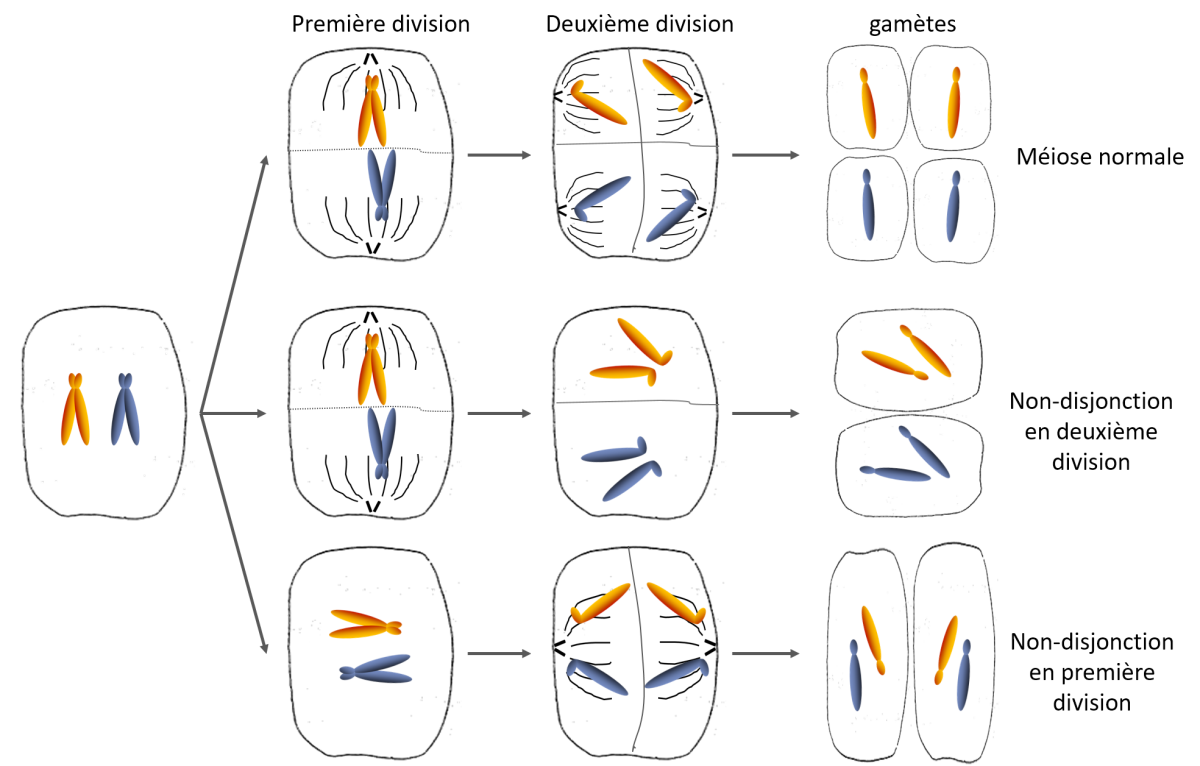
L’inégale disjonction des chromosomes de chaque
paire d’homologues en
première division de méiose ou
l’inégale disjonction des chromatides
sœurs en
deuxième division de méiose peut
aboutir à des gamètes ne possédant aucun ou deux
exemplaires de chromosome. La
fécondation avec le gamète normal aboutit alors à
l’obtention d’un individu
trisomique ou monosomique.

IV.
Comprendre
les principes de base de l’analyse génétique
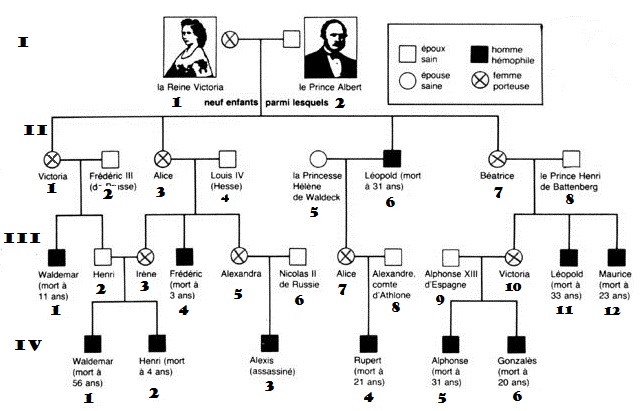
Chez
l’espèce humaine,
l’analyse génétique s’opère avant tout
au niveau de la famille. Le rescensement
des phénotypes des individus permet de construire un arbre
généalogique dont l’étude renseigne sur
le mode de
transmission de l’allèle responsable du caractère
étudié (pathologie génétique
ou non) :
· Si le caractère étudié apparaît chez un enfant alors qu’il est absent chez ses parents, l’allèle responsable est récessif, tandis que s’il est présent dans toutes les générations cet allèle est dominant. Cependant, il faut aussi considérer la probabilité d’une mutation nouvelle, apparue chez l’enfant alors que les parents ne la possèdent pas.
·
Si le
caractère étudié est
récessif mais concerne de façon beaucoup plus importante
les hommes que les
femmes, cela signifie que le gène est localisé sur le chromosome X. En effet, il suffit d’un
allèle muté pour qu’un homme
exprime le phénotype correspondant alors qu’il faudra la
réunion des deux
allèles mutés pour que la femme exprime le
caractère.
Remarque : Le cas
de gènes
situés sur les chromosomes sexuels obéit à une
logique particulière : chez
de nombreuses espèces, les femelles possèdent deux
chromosomes homologues (et
donc deux allèles pour chaque gène). Les mâles, qui
ont deux chromosomes
sexuels différents, possèdent alors certains
allèles qui ne sont présents qu’en
un seul exemplaire.
La détermination du mode de
transmission d’un allèle permet, par exemple dans le cas
d’une maladie
d’origine génétique, de procéder à
une évaluation
du risque.
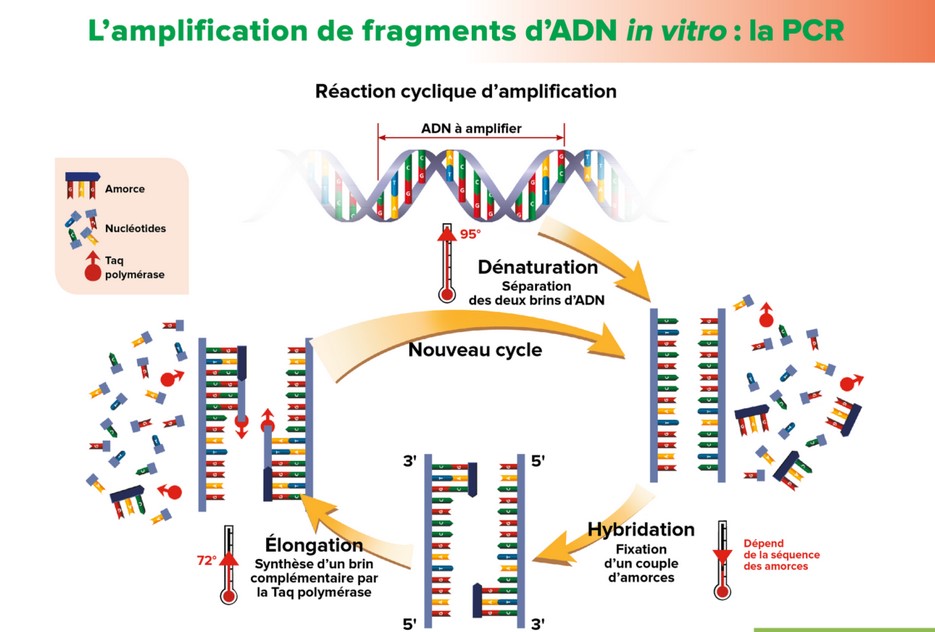
Les progrès dans le domaine
de la génétique moléculaire (techniques de
séquençage de l’ADN, PCR) permettent
un accès de plus en plus rapide et de moins en moins
coûteux aux données
génétiques individuelles. Il est ainsi possible,
grâce à des tests rapides, de
déterminer dans une famille où un risque
de maladie génétique existe quels allèles sont
présents chez les parents et
leurs enfants.
généticiens
à établir des
banques de données qui recensent tous les allèles des
gènes (plus de 2000 dans
le cas du gène CFTR impliqué dans la mucoviscidose).
Grâce aux techniques de
séquençage de l’ADN, on a accès directement
au génotype des individus.
La bio-informatique
permet aujourd’hui d’accéder à des bases de
données provenant de milliers de personnes dans le monde. Les
chercheurs
peuvent, en exploitant ces masses d’informations, relier certains
phénotypes
obsercés à des mutations précises, faisant avancer
la recherche génétique et la
prise en charge médicale des patients.

Séquence à
séquencer :
|
A |
C |
A |
G |
A |
C |
G |
A |
G |
G |
G |
C |
C |
G |
T |
A |
G |
G |
Commence la synthèse
du brin complémentaire de l’ADN à séquencer
par l’ADN polymérase.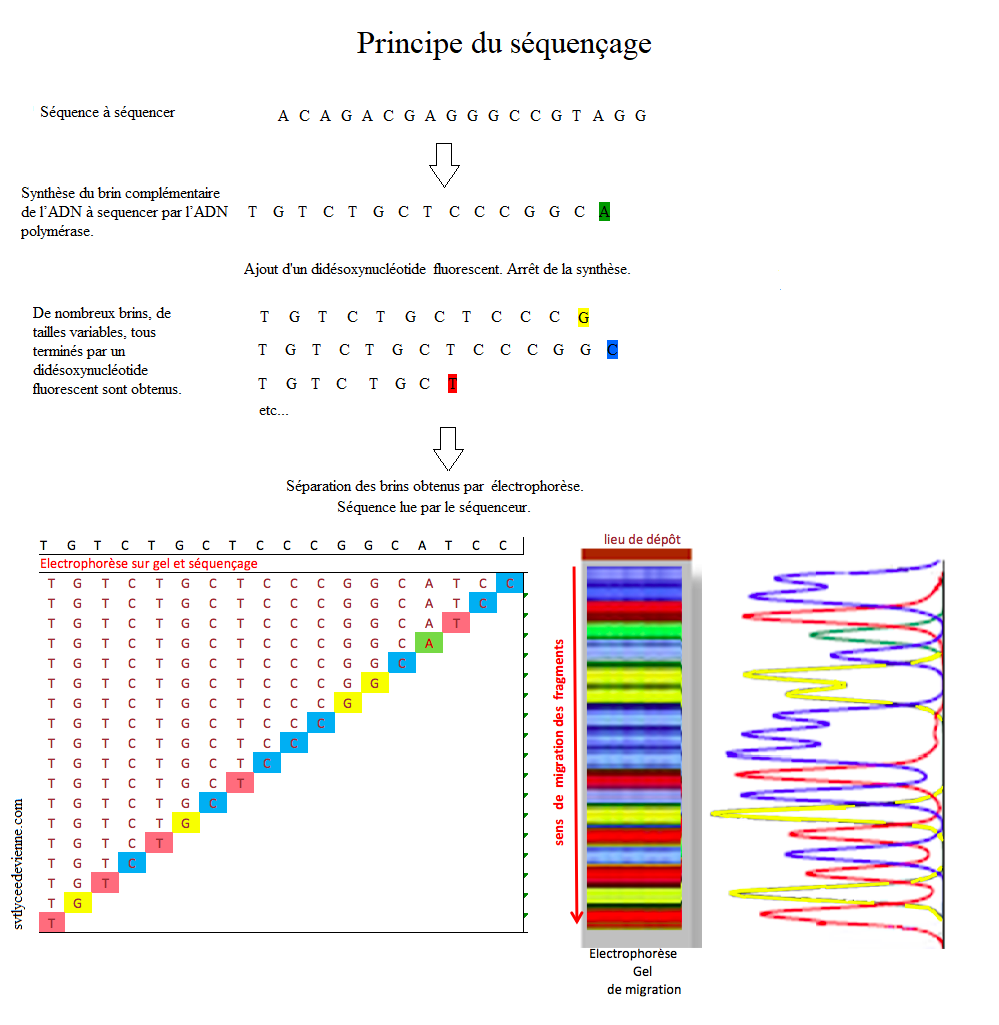
D'après
Belin (SVT Tle)